Бесплатная консультация
по тел: +7(812) 57-611-57
Консультацию можно получить в рабочий день с 10 до 16 часов по предварительной записи
Реконструктивная урология
- Методы лечения
- Диагностика
Стриктура лоханочно-мочеточникового сегмента — рубцовое сужение мочеточника приводящее к расширеню чашечно-лоханочной системы в связи с нарушением оттока мочи. Данная патология приводит повышению давления в полостной системе почки и ухудшение её функции. Любое препятствие сопровождающаяся нарушению оттока мочи приводит к гидронефрозу.
Различают первичный врожденный гидронефроз развивающийся в следствии аномалии верхних мочевыводящих путей, и вторичный приобретенный как осложнение какого-либо заболевания.
Основной причиной стриктуры ЛМС является наличие дополнительного нижнеполярного сосуда почки, который приводит к сосудисто-мочеточниковому конфликту, и образование склеротических изменений мочеточника за счет механического воздействия.
Очень часто стриктура ЛМС встречается при мочекаменной болезни, который образуется за счет механической травматизации уротелия мочеточника камнем.
Разделяют три стадии гидронефроза.
I стадия — расширение только лоханки почки.
II стадия — расширение лоханки и чашечек почки.
III стадия — выраженное истончение паренхимы почки и снижение функции органа менее чем на 20%
Чаще всего данная патология почек развивается медленно, и выявляют при плановом обследовании. Основным методом диагностики при первичном выявлении заболевания является УЗИ, где четко определяется расширение полостной системы почки и мочеточника.
Для определения более точной локализации стриктуры и оценить функцию почки выполняется экскреторная орография. Преимущество данного исследования заключается в простоте её выполнения и несет большую диагностическую ценность.
Компьютерная томография дает четкую картину данной патологии где так-же определяется функция почки, локализация стриктуры, расширение ЧЛС и самое главное визуализацию сосудов почки для определения сосудистого конфликта.
Лечения данного заболевания является только оперативным.
Существует методика эндоскопического рассечение стриктуры пиелоуретерального сегмента, который является молоинвазивным методом, что позволяет быстрому послеоперационному восстановлению пациента. Но данная методика имеет более высокий процент рецидива по сравнению с лапароскопической пластикой гидронефроза.
Чаще всего применяемым и оправданным методом оперативного лечения данного заболевания является лапароскопическая пластика лоханочно-мочеточникового сегмента. Суть данной высокотехнологичной операции заключается в том что рубцоно-измененный участок мочеточника иссекается, и накладывается новый лоханочно-мочеточниковый анастамоз перед сосудом. Интраоперационно в мочеточник устанавливается стент который позволят адекватному оттоку мочи из почки и препятствует образования мочевого затека. Через месяц в плановом порядке мочеточниковый стент удаляется.
Стриктура мочеточника – это врожденное или приобретенное уменьшение просвета мочеточника, приводящее, при длительном существовании, к нарушению оттока мочи из почки. Мочеточник – это часть мочевыделительного тракта, которая представляется собой трубку S-образной формы, соединяющую почечную лоханку и мочевой пузырь. Длина его зависит от роста человека, но в чаще всего находится в пределах 23-32 см. Просвет органа составляет 0.5-1 см, однако он неодинаков на протяжении. У здорового человека в мочеточнике имеется 3 физиологических сужения (в верхнем, среднем и нижнем отделах). Любое дополнительное сужение просвета мочеточника считается стриктурой.
По механизму возникновения стриктуры мочеточника стоит разделить на врожденные и приобретенные. Врожденные сужения мочеточника возникают вследствие наследственных аномалий (особое строение стенки мочеточника, ошибки развития плода и т.д) или из-за наличия нижнеполярного почечного сосуда и близкого расположения мочеточника к нему. Наиболее частыми факторами возникновения приобретенной стриктуры мочеточника являются: хронический воспалительный процесс почек в сочетании с мочекаменной болезнью (МКБ), ятрогенное (врачебное, лечебное) повреждение мочеточника, туберкулез органов мочевыводящих путей, вовлечение органа в опухолевый процесс, исходящий из соседних органов.
Чаще всего яркие проявления данного заболевания отсутствуют, т.к. процесс сужения просвета мочеточника может протекать длительно (месяцы, годы). Длительное существование стриктуры приводит к характерной клинической картине:
• Постоянный дискомфорт в поясничной области;
• Интенсивные периодические боли в пояснице и по ходу мочеточника;
• Частые обострения пиелонефрита (воспалительного заболевания почек);
• Появление примеси крови в моче или изменение ее прозрачности.
Для определения тактики лечения пациентов со стриктурой мочеточника важно определить протяженность суженного участка мочеточника. Для этого могут быть использованы следующие диагностические методики:
• Экскреторная (внутривенная) урография – пациенту вводится внутривенно рентген-контрастное вещество, выводящиеся почками, и производится серия рентген-снимков. Исследование позволяет оценить функцию каждой почки и проследить контуры и просвет мочеточников.
• Ультразвуковое исследование почек позволяет выявить гидронефроз (расширение полостной системы почки), наличие камней в почках, наличие острого/хронического воспаления в почке.
• Компьютерная томография (с внутривенным контрастированием) – исследование, позволяющие визуализировать почки, мочеточники, мочевой пузырь, оценить функции этих органов, наличие в них камней/опухолей. Кроме того, компьютерная томография косвенно может помочь врачу определить природу возникновения сужения мочеточника (выявить наличие нижнеполярной почечной артерии, туберкулеза, опухолей близлежащих к мочеточнику органов и д.р)
Как правило, при протяженности стриктур мочеточника более 2 см эндоскопическое лечение (бужирование сужения, эндоуретеротомия) не может быть проведено в виду крайне низкой эффективности и склонности таких стриктур к рецидивированию (повторному возникновению). В случаях, когда сужение мочеточника простирается на достаточное расстояние (более 2 см) наиболее часто применяются методики пластики мочеточника (замещения участка или всего органа окружающими тканями). Так, для замещения участка органа может быть использован аппендикс или лоскут из мочевого пузыря. Такие способы актуальны, если сужения мочеточника локализуется в нижней его трети (недалеко от мочевого пузыря). Если стриктура расположена в верхней или средней, то наиболее эффективно полное замещение мочеточника участком тонкой кишки. Лучшим клиническим и косметическим результатами обладает не открытая, а лапароскопическая кишечная пластика мочеточника (производится без разрезов, через проколы передней брюшной стенки). Такая операция является технически сложной и требует от уролога отличных мануальных навыков, обширных знаний в абдоминальной анатомии и хирургии и длительной концентрации. Кроме того, проведение подобных вмешательств в клинике невозможно без хорошо развитого диагностического звена (тщательная подготовка пациента к операции) и отделения анестезиологии и реанимации.
Лапароскопическая кишечная пластика мочеточника проводится под эндотрахеальных наркозом в сочетании со спинномозговым блоком. Суть оперативного вмешательства заключается в удалении измененного мочеточника от почечной лоханки до мочевого пузыря и замещении его участком тонкой кишки. В виду значительной технической сложности длительность данного оперативного вмешательства составляет около 4 часов и более. Безусловно, такое продолжительное пребывание пациента в «медикаментозном сне» и перенесенное им операция, требует в последствие пролонгированного пребывания в отделении реанимации для постоянного и тщательного медицинского контроля.
Недержание мочи — это непроизвольное выделение мочи из мочеиспускательного канала, не зависящее от позыва к мочеиспусканию.
Причины возникновения:
Оперативные вмешательства на предстательной железе:
Радикальная простатэктомия
Оперативное лечение аденомы предстательной железы
· Травмы головного или спинного мозга с потерей контроля над мочевым пузырем
Неврологические заболевания ( рассеянный склероз, болезнь Паркинсона)
Типы мужского недержания мочи:
Стрессовое ( непроизвольное мочеиспускание при кашле, чихании или напряжении)
· Ургентное ( непроизовольное выделение мочи, возникающее при внезапном нестерпимым позывом к мочеиспусканию)
· Смешанное ( непроизвольное мочеиспускание, сопровождающееся симптомами стрессового и ургентного типа)
Методы лечения:
Консервативное
Слинговое оперативное вмешательство
Имплантация искусственного сфинктера мочевого
В настоящее время достижения современной имплантационной хирургии позволяют решить проблему недержания мочи у мужчин в подавляющем большинстве случаев.
Искусственный сфинктер мочевого пузыря
Система контроля мочеиспускания состоит из 3 компонентов:
1. В мошонку имплантируется помпа
2. Вокруг мочеиспускательного канала фиксируется надувная манжета
3. В брюшную полость имплантируется воздушный баллон
Манжета вокруг мочеиспускательного канала надувается, тем самым препятствуя вытеканию мочи из мочевого пузыря. Для начала мочеиспускания требуется сжать имплантируемую в мошонку помпу несколько раз. Это обеспечивает выпуск жидкости из манжеты и раскрытия мочеиспускательного канала для выведения мочи
Достоинства:
· высокая эффективность (90% пациентов отмечают значительное улучшение после установления сфинктера AMS 800)
· даже в случае отдаленных осложнений или нарушений в работе сфинктера 92% пациентов считают установление сфинктера AMS Sphincter 800 оптимальным решением для себя
· 96% прооперированных пациентов рекомендуют сфинктер своим «собратьям по несчастью».
На протяжении 25 лет, которые используется искусственный сфинктер, этот метод является золотым стандартом лечения недержания мочи у мужчин
Слинговые операции выполняются мужчинам при недержании мочи после оперативных вмешательств на предстательной железе. Слинговые операции предполагают создание «слинга» (петли или гамака) из собственных тканей, синтетических или биологических материалов. Петлю из надлобкового или трансобтураторного доступа проводят под уретрой и фиксируют швами к брюшной стенке или позадилобковым структурам. Этим создается дополнительная поддержка уретре и шейке мочевого пузыря. В последнее время широкое распространение получили слинговые операции, в которых для поддержки шейки мочевого пузыря и уретры применяется самофиксирующаяся к тканям синтетическая (полипропиленовая) лента, не требующая дополнительного натяжения, так называемая свободная синтетическая петля. Эффективность операции по данным различных авторов колеблется от 40 до 80 %.
Нефроптоз – это состояние избыточной патологической подвижности почки. Здоровая почка обладает подвижностью – она способна смещаться под действием силы тяжести при вертикальном положении тела (не более 1-2 см) и при дыхании (движение диафрагмы при вдохе «толкает» почки вниз). У здорового человека существует ряд факторов, способствующих сохранению нормального положения почки в любых условиях и при любом положении тела. Связки и фасции почки, особое строение почечного ложа, паранефральная (околопочечная) жировая клетчатка и внутрибрюшное давление препятствуют смещению почки. Однако, в ряде случаев, всех вышеперечисленных факторов недостаточно, чтобы предохранить почку от избыточного смещения.
Нефроптоз чаще наблюдается у женщин в начале или середине репродуктивного возраста. Это связано с:
• гормональными особенностями строения жировой ткани;
• беременностями;
• специфическим строением соединительно-тканных волокон, делающим их более растяжимыми
• Слабым развитием мышц поясницы и передней брюшной стенки.
• Склонность к соблюдению диет, резким колебаниям веса
У мужчин нефроптоз может возникнуть при наследственных (генетических) заболеваниях соединительной ткани, в результате травм поясничной области и как проявление крайне активного образа жизни (поднятие тяжестей, прыжки с парашютом, бег на длинные дистанции).
Опасность заболевания заключается не в простом механическом опущении почки на высоту более 1 позвонка. Необходимо знать, что при смещении почки вниз происходит ее ротация (поворот вокруг оси), что дополнительно приводит к натяжению почечной ножки (почечной артерии и вены), сужению просвета почечных сосудов и значимому ухудшению кровоснабжению органа. Кроме того, стремящаяся вниз почка приводит к образованию множества «колен» в мочеточнике (мочеточник складывается и гофрируется под весом «висящей» почки). Это неизбежно ведет к нарушению отхождения мочи.
В зависимости от степени смещения нижнего полюса почки в положении стоя (1.5, 2 или 3 позвонка) выделяют разные стадии нефроптоза, и соответственно, разные их клинические проявления. Однако имеются общие симптомы, наиболее часто беспокоящие пациентов, страдающих опущением почки:
• Дискомфорт в поясничной области, усиливающийся при длительном стоянии, беге, пряжках;
• Боли в боку и в животе;
• Примесь крови в моче;
• Частые обострения воспалительного процесса в почке;
• повышение артериального давления.
Диагностируется нефроптоз с помощью комплекса исследований. Доктор может оценить наличие патологического смещения почки пальпаторно. Однако, более достоверные данные о заболевании могут быть получены с помощью:
• Ультразвуковое исследование почек позволяет выявить положение почки, наличие гидронефроза (расширение полостной системы почки), камней в почках, наличие острого/хронического воспаления в почке;
• экскреторной урографии (пациенту вводится внутривенно рентген-контрастное вещество, выводящиеся почками, и производится серия рентген-снимков. Исследование позволяет оценить положение, размеры и функцию каждой почки, а также проследить контуры мочеточника).
Важно оба исследования проводить в как в положении лежа, так и стоя!
Пациенты с нефроптозом 1 стадии могут получать консервативное лечение, заключающиеся в выполнении лечебной гимнастики, соблюдении высоко калорийной диеты, ношении бандажа, ведении «щадящего» образа жизни (нельзя поднимать тяжести, длительно ходить и бегать и т.д.). Хирургическое лечение нефроптоза проводится при далеко зашедшем заболевании, проявляющимся частыми пиелонефритами (воспалением почки), снижением почечной функции, гидронефрозом (расширением чашечно-лоханочной системы почки). Кроме того, постоянная боль в пояснице также является показанием к оперативному лечению.
Наиболее щадящим, эффективным и безопасным методом оперативного лечения является лапароскопическая нефропексия. Данная операция проводится под общим наркозом и обладает отличным косметическим результатом. Суть методики заключается в имплантации (установке) специальной медицинской сетки (протеза) в область почки, который играет роль своеобразного «гамака» Сетка подвешивает почку к поясничной мышце и не дает органу избыточно опускаться под силой тяжести. Данный протез не требует удаления, он полностью биологически инертен (не вызывает патологического ответа организма). Со временем сетка «обрастает» собственной соединительной тканью организма и формируется дополнительную защитную капсулу вокруг почки.
Лапароскопическая нефропексия производится через 3-4 прокола передней брюшной стенки, без разрезов, что позволяет значительно снизить болевые ощущения в послеоперационном периоде, по сравнению с открытой операцией. Пациенты, перенесшие данное вмешательство, на следующие сутки способны свободно передвигаться, а через 2-3 дня могут быть выписаны из клиники.
Нефроптоз – это состояние избыточной патологической подвижности почки. Здоровая почка обладает подвижностью – она способна смещаться под действием силы тяжести при вертикальном положении тела (не более 1-2 см) и при дыхании (движение диафрагмы при вдохе «толкает» почки вниз). У здорового человека существует ряд факторов, способствующих сохранению нормального положения почки в любых условиях и при любом положении тела. Связки и фасции почки, особое строение почечного ложа, паранефральная (околопочечная) жировая клетчатка и внутрибрюшное давление препятствуют смещению почки. Однако, в ряде случаев, всех вышеперечисленных факторов недостаточно, чтобы предохранить почку от избыточного смещения.
Нефроптоз чаще наблюдается у женщин в начале или середине репродуктивного возраста. Это связано с:
гормональными особенностями строения жировой ткани;
беременностями;
специфическим строением соединительно-тканных волокон, делающим их более растяжимыми
Слабым развитием мышц поясницы и передней брюшной стенки.
Склонность к соблюдению диет, резким колебаниям веса
У мужчин нефроптоз может возникнуть при наследственных (генетических) заболеваниях соединительной ткани, в результате травм поясничной области и как проявление крайне активного образа жизни (поднятие тяжестей, прыжки с парашютом, бег на длинные дистанции).
Опасность заболевания заключается не в простом механическом опущении почки на высоту более 1 позвонка. Необходимо знать, что при смещении почки вниз происходит ее ротация (поворот вокруг оси), что дополнительно приводит к натяжению почечной ножки (почечной артерии и вены), сужению просвета почечных сосудов и значимому ухудшению кровоснабжению органа. Кроме того, стремящаяся вниз почка приводит к образованию множества «колен» в мочеточнике (мочеточник складывается и гофрируется под весом «висящей» почки). Это неизбежно ведет к нарушению отхождения мочи.
В зависимости от степени смещения нижнего полюса почки в положении стоя (1.5, 2 или 3 позвонка) выделяют разные стадии нефроптоза, и соответственно, разные их клинические проявления. Однако имеются общие симптомы, наиболее часто беспокоящие пациентов, страдающих опущением почки:
Дискомфорт в поясничной области, усиливающийся при длительном стоянии, беге, пряжках;
Боли в боку и в животе;
Примесь крови в моче;
Частые обострения воспалительного процесса в почке;
повышение артериального давления.
ДИАГНОСТИКА:
Диагностируется нефроптоз с помощью комплекса исследований. Доктор может оценить наличие патологического смещения почки пальпаторно. Однако, более достоверные данные о заболевании могут быть получены с помощью:
Ультразвуковое исследование почек позволяет выявить положение почки, наличие гидронефроза (расширение полостной системы почки), камней в почках, наличие острого/хронического воспаления в почке;
экскреторной урографии (пациенту вводится внутривенно рентген-контрастное вещество, выводящиеся почками, и производится серия рентген-снимков. Исследование позволяет оценить положение, размеры и функцию каждой почки, а также проследить контуры мочеточника).
Важно оба исследования проводить в как в положении лежа, так и стоя!
ЛЕЧЕНИЕ:
Пациенты с нефроптозом 1 стадии могут получать консервативное лечение, заключающиеся в выполнении лечебной гимнастики, соблюдении высоко калорийной диеты, ношении бандажа, ведении «щадящего» образа жизни (нельзя поднимать тяжести, длительно ходить и бегать и т.д.). Хирургическое лечение нефроптоза проводится при далеко зашедшем заболевании, проявляющимся частыми пиелонефритами (воспалением почки), снижением почечной функции, гидронефрозом (расширением чашечно-лоханочной системы почки). Кроме того, постоянная боль в пояснице также является показанием к оперативному лечению.
Наиболее щадящим, эффективным и безопасным методом оперативного лечения является лапароскопическая нефропексия. Данная операция проводится под общим наркозом и обладает отличным косметическим результатом. Суть методики заключается в имплантации (установке) специальной медицинской сетки (протеза) в область почки, который играет роль своеобразного «гамака» Сетка подвешивает почку к поясничной мышце и не дает органу избыточно опускаться под силой тяжести. Данный протез не требует удаления, он полностью биологически инертен (не вызывает патологического ответа организма). Со временем сетка «обрастает» собственной соединительной тканью организма и формируется дополнительную защитную капсулу вокруг почки.
Лапароскопическая нефропексия производится через 3-4 прокола передней брюшной стенки, без разрезов, что позволяет значительно снизить болевые ощущения в послеоперационном периоде, по сравнению с открытой операцией. Пациенты, перенесшие данное вмешательство, на следующие сутки способны свободно передвигаться, а через 2-3 дня могут быть выписаны из клиники.
Недержание мочи.
В результате анализа Европейской Ассоциации Урологов было установлено, что симптомы НМ проявляются хотя бы 1 раз в год у 5–69% женщин и 1–39% мужчин. В целом НМ у женщин встречается в 2 раза чаще, чем у мужчин.
Факторы риска развития НМ у женщин
Беременность и родоразрешение через естественные родовые пути являются факторами риска, оказывающими существенное влияние на развитие НМ, однако с возрастом их влияние ослабевает. Несмотря на распространенное мнение, менопауза не является фактором риска возникновения НМ. Кроме того, имеются противоречивые данные в отношении влияния гистерэктомии на развитие НМ. По результатам большого количества исследований было установлено, что сахарный диабет – фактор риска развития НМ. Имеют значение применение пероральных эстрогенов и показатель индекса массы тела. Хотя незначительное нарушение когнитивных функций и не считается фактором риска возникновения НМ, оно влияет на степень выраженности заболевания.
Курение, диета, депрессии, инфекции мочеполовых путей и физические нагрузки не служат факторами риска.
Гиперактивный мочевой пузырь (ГАМП)
Заболеваемость ГАМП составляет 10–26% среди мужчин и 8–42 % среди женщин. Количество случаев увеличивается в соответствии с возрастом пациентов и часто сочетается с другими СНМП. Некоторые хронические состояния, такие как депрессия и запоры, неврологические заболевания и эректильная дисфункция, значительно увеличивают риск развития ГАМП (даже с учетом возраста пациента, его пола и страны проживания).
Первичное лечение НМ у женщин
Лечение стрессового, ургентного или смешанного НМ должно включать следующие компоненты:
• изменение образа жизни пациентки;
• физиотерапия;
• поведенческая терапия;
• мочеиспускание по графику;
• медикаментозное лечение
Эффективность некоторых методов лечения считается доказанной. Однако ввиду малого количества информации, рекомендации относительно других методов лечения являются недостаточно обоснованными.
Первичное лечение НМ у женщин
Рекомендации СР
Изменение образа жизни
• Снижение веса у женщин с умеренной или значительной степенью ожирения приводит к уменьшению выраженности симптомов НМ
• Снижение потребления кофеина может приводить к снижению выраженности симптомов НМ
• Снижение суточного объема потребления жидкости следует рекомендовать только тем пациенткам, которые употребляют чрезмерное количество жидкости, так как в иных случаях данное ограничение может приводить к развитию запоров, инфекции мочевыводящих путей или дегидратации организма
• Для профилактики НМ при кашле или иных индуцирующих факторах можно рекомендовать больным скрещивать ноги и наклоняться вперед
Тренировка мышц тазового дна: общие принципы
• Тренировка мышц тазового дна должна являться одним из основных методов консервативного лечения стрессового, ургентного или смешанного НМ у женщин
• Необходимо назначать настолько интенсивный курс тренировок, насколько это возможно (например, интенсивный курс тренировок и частые консультации у специалиста). Эффективность курса тренировок, разработанного специалистом, выше, чем самостоятельное выполнение упражнений. Кроме того, рекомендуется чаще консультировать больных с НМ
• Достоверные данные об увеличении эффективности от тренировок при осуществлении обратной связи путем регистрации активности мышц диафрагмы таза отсутствуют
— осуществление механизмов «обратной связи» в стационаре;
— осуществление механизмов «обратной связи» амбулаторно
Применение влагалищных конусов (конических грузов)
• Применение влагалищных конусов является одним из основных методов лечения НМ, рекомендуемых женщинам, у которых не возникает затруднений при их использовании
• При использовании влагалищных конусов может ощущаться дискомфорт или проявляются побочные реакции, вследствие чего лечение не будет эффективным
• Методы лечения стрессового и смешанного НМ с применением влагалищных конусов или назначением электростимуляции являются одинаково эффективными, однако при назначении указанных методов лечения у пациенток может отмечаться дискомфорт и проявляются побочные реакции
Электростимуляция
• Электростимуляция является методом лечения стрессового, ургентного и смешанного НМ
• Для лечения СНМ рекомендуется назначение полугодового амбулаторного курса электростимуляции с частотой 50 Гц 2 раза в день
• Эффективность от проведения низкочастотной амбулаторной электростимуляции в течение 6 месяцев оказывается выше, чем от проведения 16 сеансов высокочастотной электростимуляции в стационаре
• Для лечения ургентного НМ, обусловленного ГД, рекомендуется назначение девятинедельного амбулаторного курса электростимуляции с частотой 4–10 Гц 2 раза в день
• Данные об увеличении эффективности при проведении электростимуляции совместно с применением методик обратной связи, отсутствуют
• Метод электростимуляции применяется не всегда: в некоторых случаях име-ются противопоказания, часть женщин испытывают затруднения при назначении электростимуляции или по каким-либо иным соображениям отказываются от данного метода лечения
Магнитная стимуляция
• Эффективность магнитной стимуляции не доказана, поэтому она используется только при проведении клинических исследований
Тренировка мочевого пузыря
• Тренировка мочевого пузыря является одним из основных методов лечения ургентного НМ у женщин
• Эффективным методом лечения ургентного НМ может служить назначение М-холиноблокаторов или тренировка мочевого пузыря
• Так как при применении лекарственных препаратов могут возникать побочные эффекты, многие пациенты предпочитают тренировку мочевого пузыря как основной метод лечения
• Эффективность фармакотерапии в сочетании с самостоятельным выполнением тренировок, которым больная обучалась при прочтении кратких руководств, не превышает ее эффективности без данных тренировок
• Эффективность комбинации тренировок мышц тазового дна и мочевого пузыря при лечении женщин со стрессовым или смешанным НМ может оказаться выше, чем от отдельных тренировок мышц тазового дна
• При обучении пациентов врачи и исследователи должны рекомендовать им Не установлена специальную литературу
• Составление специального режима мочеиспускания (мочеиспускание производится с интервалом в 2 часа) может стать эффективным методом лечения женщин с незначительно выраженным НМ и неучащенным мочеиспусканием
Мочеиспускание по графику
• Составление специального режима мочеиспускания
Лечение
Если уродинамическое исследование подтверждает СНМ, обусловленное гипермобильностью уретры и шейки мочевого пузыря, рекомендованы следующие методы лечения:
• комплексное терапевтическое лечение;
• позадилонные суспензорные операции;
• операции на шейке мочевого пузыря/субуретральные слинговые операции.
Кроме того, необходимо назначать симптоматическое лечение. В случае выявления патологии
шейки мочевого пузыря рекомендуется выполнение слинговых операций, имплантация ИМС и использование периуретральных инъекций.
Методами лечения ургентного НМ (ГАМП), обусловленного идиопатической ГД, служат нейромодуляция или аугментация мочевого пузыря. При наличии резистентной к терапевтическим методам ГД, следует назначить инъекции ботулотоксина.
Причиной дисфункции мочевого пузыря, приводящей к значительному увеличению объема остаточной мочи, может являться инфравезикальная обструкция или гипоактивность детрузора. Про-лапс ОМТ также является частой причиной нарушения мочеиспускания.
Хирургическое лечение НМ у женщин
Достоверная информация о частоте развития осложнений после выполнения оперативного вмешательства по поводу НМ отсутствует, что связано с недостатком стандартизированных методов оценки результатов исследований. Кроме того, дан-ные о частоте возникновения осложнений, полученные в ходе научных исследований, отличаются от дан-ных, полученных в повседневной практике. Однако вероятность возникновения осложнений, по всей ви-димости, относительно невелика. В национальной статистической базе данных содержится информация о частоте осложнений, при анализе которой удалось выявить, что данный показатель снижается в том случае, если хирургическое лечение проводится опытным специалистом (уровень доказательности 2–3). Опытным считается специалист, выполняющий за 1 год не менее 20 оперативных вмешательств по по-воду одного патологического состояния (Национальный институт повышения квалификации (NICE)).
Хирургические методы лечения НМ у женщин
Хирургический метод УД СР
Передняя кольпорафия
• Данный метод лечения не менее эффективен, чем игольчатая суспензия. Однако эффективность передней кольпорафии ниже открытой кольпосуспензии. Положительный эффект от операции со временем ослабевает
• Передняя кольпорафия не рекомендована как метод только для лечения СНМ
Открытая кольпосуспензия
• Эффективность открытой кольпосуспензии сопоставима с эффективностью операции по имплантации ретропубикального слинга
• Открытая кольпосуспензия также эффективна, как и операция по имплантации слинга в области шейки мочевого пузыря
• Открытая кольпосуспензия также эффективна, как и трансобтураторная имплантация слинга
• После выполнения кольпосуспензии риск развития дисфункции мочеиспускания выше, чем после проведения операции TVT
• Риск развития дисфункции мочеиспускания после кольпосуспензии ниже, чем риск после слинговой операции
• Пролапс ОМТ после выполнения операции TVT возникает реже, чем после кольпосуспензии
• Риск возникновения ГД после кольпосуспензии такой же, как и риск после выполнения операции TVT
• При неосложненных формах СНМ не рекомендуется выполнять уретропластику с использованием принципа Митрофанова, имплантацию
слингов в области шейки мочевого пузыря, пластику влагалища
• Открытая кольпосуспензия является эффективным методом лечения первичного СНМ (после операции отмечается долгосрочный положительный эффект)
Лапароскопическая кольпосуспензия
• В том случае, если лапароскопическая кольпосуспензия выполняется опытным хирургом, эффективность данного метода лечения равна таковой при открытой кольпосуспензии
• Эффективность лапароскопической кольпосуспензии равна или выше эффективности лечения при проведении операции TVT
• Выполнение лапароскопической кольпосуспензии занимает меньше времени, чем выполнение операции имплантации TVT. Кроме того реабилитационный период после выполнения лапароскопической кольпосуспензии короче
• Лапароскопическая кольпосуспензия служит методом лечения СНМ В
• Данная операция должна выполняться только опытными лапароскопическими хирургами
Классические слинговые операции
• Эффективным методом лечения является имплантация аутологичных фасциальных слингов
• Эффективность лечения при имплантации аутологичных фасциальных слингов выше, чем при имплантации слингов из биологических или синтетических материалов
• Имплантация аутологичного фасциального слинга является эффективным методом лечения СНМ. После выполнения операции отмечается длительный положительный эффект
Периуретральные инъекции
• В ходе исследований было установлено, что эффективность при использовании периуретральных инъекций равна таковой при аутотрансплантации жировой ткани или при лечении плацебо
• Эффективность указанного метода лечения ниже, чем у традиционных хирургических вмешательств
• Эффективность лечения не зависит от материала для инъекции 2
• Сравнительных исследований эффективности лечения с малоинвазивными или нехирургическими методами лечения не проводилось
• Перед применением метода следует предупреждать пациенток о том, что:
– положительный эффект со временем снижается;
– может потребоваться проведение повторного курса инъекций;
– существуют более эффективные хирургические методы лечения
Петли, помещаемые на среднюю часть уретры
• Эффективность слинговой операции TVT выше эффективности операции SPARC
• Операции IVS и TVT являются одинаково эффективными, однако после первой чаще возникают осложнения
Сравнение операций по имплантации петель, помещаемых на среднюю часть уретры, с другими хирургическими методами лечения
• Эффективность TVT, кольпосуспензии и традиционных слинговых операций примерно одинакова
• Операция TVT требует больше времени, чем кольпосуспензия. Сроки пребывания в стационаре и реабилитации после операции TVT также короче, чем после кольпосуспензии
• После кольпосуспензии чаще отмечаются проблемы, связанные с мочеиспусканием, и может развиться пролапс ОМТ
Сравнение позадилонных и трансобтураторных слинговых операций
• В течение 12 месяцев после выполнения операций отмечается одинаковая эффективность
• В ходе ряда исследований было установлено, что частота осложнений, возникающих после выполнений операций, одинакова
• Риск повреждения мочевого пузыря в 6 раз выше при выполнении позадилонных слинговых операций, чем при выполнении трансобтураторных слинговых операций
• Риск повреждения уретры в 4 раза выше при выполнении трансобтураторных слинговых операций, чем при позадилонных операциях
Противопоказания к имплантации петель, помещаемых на среднюю часть уретры
• Абсолютными противопоказаниями являются:
— наличие уретро-влагалищного свища;
— наличие дивертикула уретры;
— повреждение уретры в ходе операции;
— злокачественное опухолевое поражение органов мочевыделительной системы
• Риск осложнений возрастает при:
– предшествующей ЛТ;
– наличии инфекций мочевыделительной системы;
– применении стероидов;
– хронической обструктивной болезни легких;
– приеме антикоагулянтов;
– атрофии влагалища;
– врожденных патологиях (экстрофия, уретральная эктопия и т. д.);
– беременности
Мини-слинги
• Недостаточно данных
Хирургические операции по поводу ГД
• Крестцовая нейромодуляция является эффективным методом лечения ургентного НМ, а также императивных позывов и учащенного мочеиспускания
• Эффективным методом лечения является стимуляция большеберцового нерва, однако длительность положительного эффекта не установлена
Дивертикул уретры
• Рекомендации степени А по поводу диагностики и лечения СНМ при наличии дивертикула уретры отсутствуют
• При проведении долгосрочного исследования было установлено, что рецидив дивертикула отмечается в 17% случаев; при дивертикуле СНМ возникает в 38% случаев, а диспареуния – в 22% случаев
Образование свища мочевыделительной системы (неакушерская патология)
• Рекомендации степени А по поводу диагностики патологии, сроках выполнения оперативного вмешательства, выбора методики лечения и дополнительных методов лечения, отсутствуют. Рандомизированных и/или контролируемых исследований практически не проводилось
Степень рекомендации хирургического лечения СНМ
Хирургическая процедура СР
• Передняя кольпорафия
• Трансвагинальная иммобилизация шейки мочевого пузыря (игольчатая суспензия) Отсутствует
• Кольпосуспензия по Burch
• Кольпосуспензия по Burch (лапароскопическая, выполняется только опытными хирургами)
• Паравагинальная пластика
• Уретропластика по Marshall-Marshetti-Krantz
• Имплантация аутологичного фасциального слинга в области шейки мочевого пузыря
• Имплантация субуретрального слинга (TVT)
• Использование периуретральных инъекций
Стриктура уретры (стриктурная болезнь уретры) — это рубцовое сужение ее просвета, приводящее к нарушениям мочеиспускания (дизурия) в виде слабости струи мочи, ее раздвоения, разбрызгивания и неполного опорожнения мочевого пузыря с развитием хронической и в некоторых случаях острой задержки (ретенции) мочи.
Стриктуры уретры имеют склонность к рецидивированию и высокой частоте
развития эректильной дисфункции, нарушений функций мочевого пузыря и почек, что является сложной медико-социальной проблемой.
Различают врожденные и приобретенные стриктуры уретры.
По причине образования различают поствоспалительные, химические и посттравматические стриктуры. В настоящее время наиболее часто встречаются посттравматические стриктуры и облитерации (заращения) уретры.
При наличии облитерации уретры самостоятельное мочеиспускание становится невозможным, такому больному для отведения мочи накладывается постоянный надлобковый мочепузырный свищ, в котором установлен специальный катетер.
Диагноз стриктуры мочеиспускательного канала устанавливают при помощи уретрографии (введение контрастного вещества в мочеиспускательный канал или в вену). Также дополнительно используют эндоскопические методы диагностики-уретроцистоскопию, УЗИ, МРТ.
Лечение может быть консервативным и оперативным.
Консервативное заключается в проведении сеансов бужирования уретры. Оно используется при коротких (не более 1 см) сужениях. Бужирование заключается в проведении специально разработанных для этой цели жестких инструментов, которые называются бужами, через рубцово-суженные участки мочеиспускательного канала с целью расширения просвета уретры в зоне стриктуры. Чтобы буж проходил легче, а болевые ощущения были менее интенсивными, в уретру вводят специальный гель с анестетиком (катеджель). В ряде случаев применяют наркоз. Бужирование уретры требует осторожности, так как выполняется вслепую, и может сопровождаться осложнениями. Бужирование дополняют назначением противовоспалительных и рассасывающих препаратов.
Хирургическое лечение.
Операцию выполняют эндоскопическим (без разреза кожных покровов) или открытым методом. Эндоскопическая операция заключается во внутренней оптической (под контролем зрения) уретротомии-рассечения сужения уретры при помощи так называемого «холодного» ножа или лазера. Ее применяют при непротяженных (до 2 см), в том числе множественных сужениях мочеиспускательного канала. Она является нерадикальным вмешательством, так как рубцовая ткань полностью не удаляется, вследствие чего имеет место довольно высокий процент рецидивов. Данный метод широко используется большинством урологов, т.к. не во всех центрах выполняются реконструктивные операции на уретре.
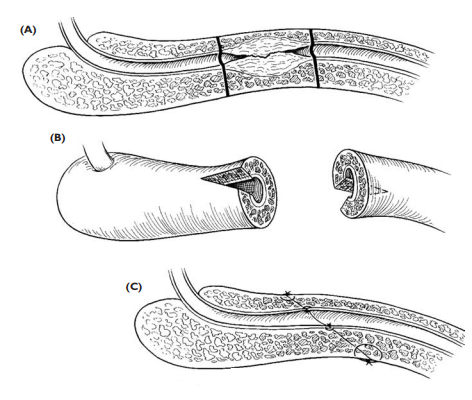
Радикальным методом лечения сужений и облитераций является открытое иссечение (резекция) уретры. Операция заключается в полном иссечении рубцовой ткани и сшивании неизмененных ее концов-анастомотическая уретральная реконструкция. Эта операция легко выполнима при локализации сужения в бульбозном отделе мочеиспускательного канала (резекция уретры по Хольцову). Значительно сложнее произвести оперативное лечение стриктур задней уретры, для чего используются специальный инструментарий и техника оперативного вмешательства.
Анастоматическая пластика уретры
Данный вид операции не применяется при стриктурах висячего отдела уретры, так как в подавляющем большинстве случаев имеет место значимое укорочение длины полового члена.
При более протяженных сужениях, а также при стриктурах висячей уретры выполняют кожную (лоскутную) или буккальную (участком слизистой оболочки щеки) пластику уретры, разделенную в некоторых случаях на два этапа-аугментационная и заместительная уретральная реконструкция.
Буккальная пластика уретры
В городском центре эндоскопической урологии и новых технологий для лечения стриктурной болезни уретры используются как эндоскопические (внутренняя оптическая уретротомия «холодным ножом» или лазером), так и радикальные открытые вмешательства (резекция уретры с концевым анастомозом (операция Хольцова), замещение участка сужения уретры лоскутами из слизистой оболочки щеки, губы и языка пациента (буккальная пластика), а также пластика кожными лоскутами). Вышеуказанные операции позволяют добиться нормализации акта мочеиспускания, избавления пациента от наличия постоянного катетера в полости мочевого пузыря и связанной с ним инфекцией мочевыводящих путей, а также восстановления эректильной функции в большинстве случаев.
Однако, несмотря на положительные результаты вышеприведенных способов оперативного лечения, больные с сужениями мочеиспускательного канала должны находиться под постоянным наблюдением уролога в связи с риском повторного сужения просвета уретры.
Эпидемиология и факторы риска
Эрекция – нейроваскулярный феномен, связанный с гормональным контролем, включающий артериальную дилатацию, расслабление гладкой трабекулярной мускулатуры и активацию корпоровеноокклюзи-онного механизма.
ЭД определяется как постоянная неспособность достичь и поддерживать эрекцию, достаточную для успешного полового акта. Несмотря на то, что ЭД не представляет опасности для жизни, она затрагивает физическое и психическое здоровье, а также оказывает значительное влияние на качество жизни самого пациента (QoL) , его партнерши и членов семьи.
Эпидемиология
Полученные в последнее время эпидемиологические данные указывают на высокую распространенность и частоту возникновения ЭД по всему миру. Первое широкомасштабное исследование ЭД на уровне сообщества было проведено в Массачусетсе (MMAS – массачусетское исследование среди пожилых мужчин). По данным исследования, в США общая распространенность возникновения ЭД среди мужчин в возрасте 40–70 лет, не обращавшихся в стационар, составила 52% в Бостоне и прилегающей к нему территории; специфическая распространенность минимальной, умеренной и полной ЭД составила 17,2; 25,2 и 9,6% соответственно. В исследовании в Кельне среди мужчин 30–80 лет частота выявления ЭД составила 19,2%, причем этот показатель, связанный с возрастом, увеличивался от 2,3 до 53,4%. В ходе исследования National Health and Social Life Survey (NHSLS) выявлено, что распространенность нарушения сексуальной функции (помимо ЭД) составила 31%. Показатель заболеваемости ЭД (новых случаев в год на 1000 мужчин) составил 26 в исследовании MMAS, 65,6 (при медиане наблюдения до 2 лет) – в исследовании в Бразилии и 19,2 (при медиане наблюдения 4,2 года) – в исследовании в Дании. Разрыв между данными этих исследований можно объяснить различиями в методах их про-ведения и возрасте участников, а также социально-экономическом статусе исследуемых популяций.
Факторы риска
Факторы риска возникновения ЭД аналогичны таковым для сердечно-сосудистых заболеваний (например, отсутствие физических упражнений, тучность, курение, гиперхолестеринемия, метаболический синдром), некоторые из них могут изменяться. В исследовании MMAS у мужчин, начавших заниматься спортом в середине жизни, выявлены снижение риска возникновения ЭД на 70% по сравнению с мужчинами, ведущими сидячий образ жизни, а также более низкая частота возникновения ЭД в течение 8 лет последующего динамического наблюдения. В многоцентровом рандомизированном открытом исследовании сравнивали тучных мужчин с умеренной ЭД, которые занимались спортом на протяжении 2 лет и снизили массу тела, с контрольной группой, относительно которой представлена общая информация о выборе здоровой пищи и физических упражнений. Значительные улучшения в группе с изменением образа жизни выявили значительное улучшение индекса массы тела, показателей физической активности, а также ЭД. Эти изменения были в высокой степени связаны со снижением массы тела и уровнем физической активности. Тем не менее необходимо провести контролируемые проспективные исследования, чтобы установить степень влияния физических упражнений или других изменений образа жизни в отношении профилактики и лечения ЭД.
Возникновение ЭД после радикальной простатэктомии
Радикальная простатэктомия – РПЭ (в любой форме: открытая, лапароскопическая или роботоассисти-рованная) – широко распространенная процедура, проводимая пациентам при клинически локализо-ванном раке простаты (PCa) и ожидаемой продолжительностью жизни не менее 10 лет. Эта процедура может привести к специфическим последствиям лечения, которые влияют на качество жизни. Значение данного фактора в последнее время возросло, потому что рак простаты выявляется все чаще у молодых пациентов. Исследование показало, что у 25–75% мужчин после операции возникает ЭД.
ЭД после простатэктомии – многофакторное заболевание. Повреждение кавернозного нерва вызывает в пещеристых телах проапоптотические (потеря гладкомышечной ткани) и профиброзные (увеличение содержания коллагена) изменения. Эти изменения могут быть также вызваны недостатком кислорода и слабым притоком крови к кавернозному телу.
Причины возникновения ЭД
Васкулогенная
• Сердечно-сосудистая патология
• Гипертония
• Диабет
• Гиперлипидемия
• Курение
• Обширное хирургическое вмешательство (РПЭ) или лучевая терапия (области таза или забрю-шинного пространства)
Нейрогенная
Центральные причины
• Множественный склероз
• Множественная атрофия
• Болезнь Паркинсона
• Опухоли
• Инсульт
• Патология межпозвоночных дисков
• Заболевания спинного мозга
Периферические причины
• Диабет
• Алкогольная зависимость
• Уремия
• Полиневропатия
• Хирургическое вмешательство (в области таза или забрюшинном пространстве, РПЭ)
Анатомическая или структурная
• Болезнь Пейрони
• Перелом полового члена
• Врожденное искривление пениса
• Микропенис
• Гипоспадия, эписпадия
Гормональная
• Гипогонадизм
• Гиперпролактинемия
• Гипер- и гипотиреоз
• Болезнь Кушинга
Вызванная лекарственной терапией
• Антигипертензивные препараты (диуретики и бета-блокаторы – наиболее распространенные причины)
• Антидепрессанты
• Нейролептические препараты
• Антиандрогенные препараты
• Антигистаминные препараты
• Наркотические средства (героин, кокаин, метадон)
Психогенная
• Генерализованный тип (например, недостаток сексуального возбуждения и трудности при интимной близости)
• Ситуационный тип (например, связанная с партнершей, внешней обстановкой, затрудняющей совершение полового акта, или стрессом)
Терапия 1-й линии
Терапия пероральными лекарственными препаратами
Энзим ФДЭ-5 гидролизует циклический гуанозинмонофосфат (цГМФ) в кавернозной ткани пениса. Подавление ФДЭ-5 стимулирует кровоток в пенисе, что приводит к расслаблению гладкой мускулатуры, расширению кровеносных сосудов и эрекции [30].
На сегодняшний день на рынке существует 3 потенциально селективных ингибитора ФДЭ-5, одобренных Европейским агентством лекарственных средств (EMEA) и Управлением США по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для лечения ЭД. Они не инициируют эрекцию, а требуют наличия сексуальной стимуляции для эректильного ответа.
Терапия 2-й линии
При неэффективности пероральных препаратов могут применяться интракавернозные инъекции. Частота их эффективности высокая (85%). Интракавернозное применение вазоактивных препаратов было первым методом лечения ЭД, использовавшимся более 20 лет назад.
Терапия 3-й линии (протезирование полового члена)
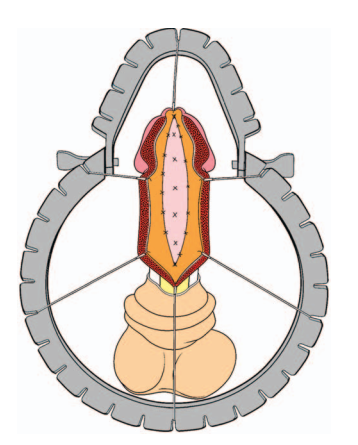
При неэффективности фармакотерапии или в случае предпочтения пациентом решения проблемы на длительный срок рассматривается хирургическая имплантация протезов полового члена. Существует 2 типа протезов: гибкие (полужесткие) и надувные (2- или 3-компонентные).
Большинство пациентов предпочитают 3-компонентные протезы в силу достижения более «естественной» эрекции.
Тем не менее 2-компонентные надувные протезы могут быть надежным вариантом выбора, у них менее сложная механика и их легче имплантировать. Полужесткий протез позволяет достичь постоян-ной устойчивой эрекции и подходит пожилым пациентам, вступающим в сексуальные отношения часто. Надувные протезы отличаются высокой стоимостью. В ряде стран пациенты получают денежную компенсацию за установку протезов при условии, если у них выявлена органическая причина ЭД и необратимая импотенция.
Имплантация протеза полового члена имеет наиболее высокие показатели эффективности (70– 87%).
Стриктура мочеточника – это врожденное или приобретенное уменьшение просвета мочеточника, приводящее, при длительном существовании, к нарушению оттока мочи из почки. Мочеточник – это часть мочевыделительного тракта, которая представляется собой трубку S-образной формы, соединяющую почечную лоханку и мочевой пузырь. Длина его зависит от роста человека, но в чаще всего находится в пределах 23-32 см. Просвет органа составляет 0.5-1 см, однако он неодинаков на протяжении. У здорового человека в мочеточнике имеется 3 физиологических сужения (в верхнем, среднем и нижнем отделах). Любое дополнительное сужение просвета мочеточника считается стриктурой.
По механизму возникновения стриктуры мочеточника стоит разделить на врожденные и приобретенные. Врожденные сужения мочеточника возникают вследствие наследственных аномалий (особое строение стенки мочеточника, ошибки развития плода и т.д) или из-за наличия нижнеполярного почечного сосуда и близкого расположения мочеточника к нему. Наиболее частыми факторами возникновения приобретенной стриктуры мочеточника являются: хронический воспалительный процесс почек в сочетании с мочекаменной болезнью (МКБ), ятрогенное (врачебное, лечебное) повреждение мочеточника, туберкулез органов мочевыводящих путей, вовлечение органа в опухолевый процесс, исходящий из соседних органов.
Чаще всего яркие проявления данного заболевания отсутствуют, т.к. процесс сужения просвета мочеточника может протекать длительно (месяцы, годы). Длительное существование стриктуры приводит к характерной клинической картине:
• Постоянный дискомфорт в поясничной области;
• Интенсивные периодические боли в пояснице и по ходу мочеточника;
• Частые обострения пиелонефрита (воспалительного заболевания почек);
• Появление примеси крови в моче или изменение ее прозрачности.
Для определения тактики лечения пациентов со стриктурой мочеточника важно определить протяженность суженного участка мочеточника. Для этого могут быть использованы следующие диагностические методики:
• Экскреторная (внутривенная) урография – пациенту вводится внутривенно рентген-контрастное вещество, выводящиеся почками, и производится серия рентген-снимков. Исследование позволяет оценить функцию каждой почки и проследить контуры и просвет мочеточников.
• Ультразвуковое исследование почек позволяет выявить гидронефроз (расширение полостной системы почки), наличие камней в почках, наличие острого/хронического воспаления в почке.
• Компьютерная томография (с внутривенным контрастированием) – исследование, позволяющие визуализировать почки, мочеточники, мочевой пузырь, оценить функции этих органов, наличие в них камней/опухолей. Кроме того, компьютерная томография косвенно может помочь врачу определить природу возникновения сужения мочеточника (выявить наличие нижнеполярной почечной артерии, туберкулеза, опухолей близлежащих к мочеточнику органов и д.р)
С тех пор, как лечение стриктур мочеточников ограничивалось исключительно открытыми хирургическими техниками, прошло много времени. Технический прогресс, ускоренный ритм жизни и возросшее внимание к экономической стороне лечебного процесса привели к тому, что в настоящее время лечение пациентов со стриктурами мочеточников невозможно представить без использования малоинвазивных технологий. Сужения мочеточника менее или равные 2.0 см принято считать непротяженными, то в этом случае возможна эндоскопическая (через просвет органов мочевыводящих путей) их коррекция. Если протяженность суженного участка мочеточника более 2 см – то наиболее оптимально выполнение лапароскопической (без проколов, через проколы передней брюшной стенки) пластики мочеточника.
Эндоскопическое лечение пациентов с сужениями мочеточника все чаще применяется во всем мире. Для такой популярности есть несколько причин. Так, по сравнению с открытыми методами лечения стриктур мочеточника эндоскопические техники имеют меньшую продолжительность операции и длительность госпитализации, более низкие показатели смертности. Более того, неудачная попытка эндоскопического лечения стриктуры не исключает возможности дальнейшего использования открытой техники операции, что позволяет считать эндоскопические методики «первой ступенью» в ведении больных с сужениями мочеточника.
Любое эндоскопическое рассечение сужения мочеточника проводится под анестезией (наркозом) в стенах операционной. В начале оперативного вмешательства выполняется цистоскопия (осмотр полости мочевого пузыря, выполняемый специальным оптическим инструментом через мочеиспускательный канал). Затем снизу-вверх осматривается мочеточник, в котором имеется сужение. При достижении стриктуры мочеточника она осматривается, определяется ее протяжение и состояние окружающих участков мочеточника. Затем суженный участок рассекается/расширяется. После процедуры в мочеточник ставится специальный эндопиелотомический стент – трубка, проходящая по всей длине мочеточника от почки до мочевого пузыря, которая играет роль каркаса для заживления мочеточника. Стент устанавливается на срок от 4 до 8 недель.
Современный арсенал конкретных эндоскопических методов коррекции стриктуры мочеточника очень большой. С успехом могут применяться:
• Бужирование (механического расширения) суженного участка мочеточника;
• Эндоуретеротомия (внутрипросветное рассечение сужения мочеточника) «холодным» ножом — т.е. специальным скальпелем или кожницами;
• Эндоуретеротомия с помощью лазерной энергии (используется специальный экстра-мощный медицинский лазер);
• Эндоуретеротомия электрической энергией (срезание внутреннего рубца мочеточника с помощью электрической петли).
К сожалению, несмотря на различные модификации рассечения стриктур мочеточников, основной их недостаток един – это рецидив (повторное возникновение) патологического процесса с формированием рубца в стенке мочеточника. Однако, при правильной оценке показаний и противопоказаний к проведению оперативного вмешательства, взвешенном выборе оптимального метода рассечения суженного участка мочеточника, оптимальной подготовке пациента к операции – успешность эндоскопических методов достигает 85-95% процентов.
Раздел находится в стадии наполнения...
Современное оборудование
Наш центр оснащен только современным оборудованием.
Строгий контроль чистоты в операционной. Постоянное повышение квалификации сотрудников и развитие центра.
Задайте вопрос специалисту:
Огромная благодарность за отношение, внимание и проведение процедуры цистоскопии доктору Корневу Кириллу Васильевичу. Какое счастье, что у нас есть такие врачи. Спасибо Вам, Кирилл Васильевич, от всей души!
Читать все отзывы
Читать все отзывы